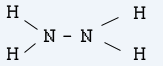Частично окисление на амоняк (NH3) води до получаване на хидразин.
2NH3 NaOCl –> N2H4 H2O NaOH
Хидразинът представлява безцветна, димяща на въздуха течност (т.т. 1,4°С ; т.к. 113,5°С )
Хидразинът и водните му разтвори се използват като редуктори при което се окислява до азот.
HO2 CH3N2H2 –>